Ele é conhecido por sua alta complexidade patogênica, estando presente em grande parte dos países. Esta enfermidade está relacionada com transtornos do sistema reprodutivo, além de afetarem os sistemas respiratório, digestório, circulatório, imunológico, linfático e outros. Seus sintomas são difíceis de serem percebidos, devido aos poucos sinais clínicos que são apresentados. A BVD é a doença que causa maior perdas econômicas em sua propriedade, superando soma das perdas causadas por outras enfermidades. Além disso, a BVD baixa severamente a imunidade dos animais, abrindo a porta para outras doenças e causando grande perda de produção
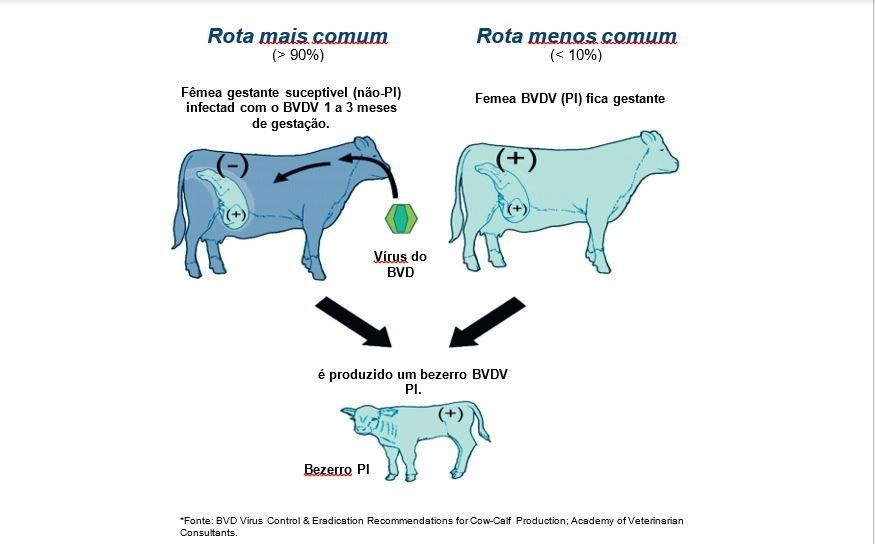
A principal característica do vírus da diarreia viral bovina (BVDV) é a capacidade de induzir infecção fetal persistente, que ocorre até o primeiro terço da gestação, vindo a gerar um animal persistentemente infectado (PI). Nessa fase da gestação, o sistema imunológico do feto é imaturo e as proteínas virais são reconhecidas erroneamente como próprias. O animal PI torna-se imunologicamente tolerante ao BVDV, e por meio deste o vírus é mantido na população bovina. A rota mais comum é quando a fêmea gestante entra em contato com o vírus nos primeiros 125 dias de gestação e a menos comum são bezerros PIs oriundos de suas mães PIS.
Num rebanho infectado pelo BVDV, existem duas fontes potenciais de infecção: o bovino PI e o bovino que está na fase aguda da enfermidade, denominado transitoriamente infectado (TI). No aspecto epidemiológico, os bovinos PI são considerados a principal fonte de infecção, porque eliminam por toda sua vida uma grande quantidade de vírus em secreções e excreções. A eliminação do vírus pelos animais TI geralmente dura poucos dias ou eventualmente semanas, porém esses animais podem promover a permanência do vírus no rebanho na ausência de animais PI interferindo, assim, nas estratégias para o controle da enfermidade.
A prevalência de bovinos PI nos rebanhos infectados pode variar de 0,5% a 2%, e entre os bovinos jovens, pode ser até o dobro. A taxa de letalidade dos bezerros PI é maior que 50% no primeiro ano de vida, principalmente porque muitos deles nascem prematuros , fracos, letárgicos ou apresentam algum tipo de malformação congênita. Alguns bezerros morrem após poucos dias ou até mesmo algumas horas após o nascimento. Aqueles que sobrevivem podem apresentar atraso no crescimento e baixa resistência a outras enfermidades, advinda de alterações funcionais de linfócitos e neutrófilos, que causam a imunossupressão. Vale ressaltar que todos animais abortados, natimortos ou nascido PI sempre são fontes de infecção por BVDV.
Muitos animais PI podem ser clinicamente saudáveis, embora a expectativa de vida seja baixa, pois todos apresentam o risco de desenvolver a doença das mucosas. Alguns podem até alcançar a idade adulta, e caso isso ocorra com fêmeas PI, a sua progênie também será PI. Desta forma, famílias de animais PI podem desenvolver-se dentro do rebanho pela transmissão do vírus nos estágios iniciais de gestação.
Outra forma de se introduzir ou manter constante a presença de animais PIs no rebanho é através da aquisição de animais de terceiros originários de fazendas positivas para PIs. Dado ao não uso do diagnostico como prática de rotina, existe uma probabilidade maior ou menor de se ter um PI no rebanho que está diretamente relacionada ao numero de bezerros ou outros animais adquiridos versus ao nível de prevalência de PI na propriedade de origem.
A patogenia do BVDV sobre a reprodução não se limita apenas a abortos ou malformações congênitas, mas também está associada a perda embrionária precoce, nos primeiros dias de vida do embrião e até mesmo durante a fecundação. Os efeitos do BVDV são verificados nas alterações da dinâmica ovariana e no comprometimento transitório da fertilidade, podendo infectar o ovário e permanecer nele por até 60 dias, ocasionando ovarite e, consequentemente, ausência de ovulação, principalmente em novilhas. Alterações inflamatórias também são encontradas no oviduto e na mucosa uterina. Nos touros, os efeitos da infecção estão relacionados aos defeitos morfológicos dos espermatozoides, à baixa qualidade do sêmen, com diminuição da mobilidade e da concentração espermática.
Diante destes aspectos é de extrema importância a associação de ferramentas de diagnostico com programas de vacinação no processo de erradicação e controle da BVD. É esta a estrategia que países da Europa e EUA tem adotado e conseguido ótimos resultados sanitários e econômicos, como melhorias quanto a fertilidade, saúde dos bezerros, ganho de peso, aumento na produção de leite, redução de tratamentos, menor incidência de problemas respiratórios, uniformidade do lote, eficiência alimentar, diminuição de infecções secundárias e melhor resposta aos programas de vacinação e bem-estar animal.
Os programas de uma maneira geral contemplam algumas fases que são a determinação do perfil sorológico da propriedade, usando o teste de BVD Ac (anticorpo), seja por amostras do tanque de leite ou do sangue das diferentes categorias de animais. Posteriormente, caso haja indicativos de desafio de campo inicia-se o teste de BVD Ag (antígeno) para a identificação do(s) animal(ais) PIs, iniciando por todos os recém-nascidos, bezerros mortos e introduções de animais e posteriormente as demais categorias. Estes uma vez identificados deverão ser eliminados da propriedade. Paralelo a este procedimento deve-se estabelecer um programa de vacinação a fim de que se minimize os riscos de nascimento de novos animais PIs e também prover uma redução das sintomatologias clinicas.
Uma vez implantado o programa, este deve ser contínuo e ter por base a vigilância e a biossegurança, a fim de impedir que se adentre na propriedade animais potencialmente positivos oriundos de propriedades que não fazem o uso desta prática.
O BVD é causa de varias perdas em qualquer sistema produtivo seja ele de corte, leite e confinamento. Estima-se que um animal PI seja capaz de contaminar cerca de 60-70% do rebanho. Ter um PI em um rebanho é como vacinar os mesmos diariamente. No entanto, estes animais terão que responder imunologicamente e isto requer uma energia a mais, o que gerará uma diminuição na produção de carne, leite, ou seja perda na eficiência produtiva e reprodutiva. O sucesso de um programa de BVDV está em identificar e eliminar o animal PI, ter um bom programa de biossegurança e vigilância com o uso constante do diagnostico.
Teste IDEXX para detecção do BVDV
A IDEXX possui mais de 20 anos de experiência em programas de erradicação de BVDV em diferentes países como Alemanha, Suíça, França, Reino Unido, Inglaterra, Irlanda e outros, oferecendo a opção mais rápida e confiável disponível no mercado, sendo a única tecnologia que detecta porção Erns da proteína viral e Genótipos 1, 2.
A IDEXX dispõem dos seguintes testes:
– IDEXX BVDV Ag/Serum Plus Test– Teste de ELISA utilizado para se detectar os animais PIs em amostras de sangue e orelha.
– RealPCR BVDV RNA Mix– Teste de PCR utilizado para se detectar os animais PIs em amostras de sangue e orelha.
– IDEXX BVDV Total Ab Test– Teste de ELISA utilizado para se detectar a presença de anticorpos seja em amostras de leite ou sangue.
Caracteristicas:
– É o único teste que detecta porção Erns da proteína viral
– Detecta Genótipos 1, 2
Para saber mais, entre em contato com a equipe técnica da IDEXX Brasil: 0800 404 3399 ou e-mail vendasbrasil@idexx.com
REFERÊNCIAS
Bartlett B., Grooms, D. BVD-PI eradication: unintended consequences. Michigan Dairy Review. 2008;13(3). Available at: https://www.msu.edu/user/mdr/vol13no3/vol13no3.pdf.
Fourichon C, F Beaudeau, N Bareille, H Seegers. 2005. Quantification of economic losses consecutive to infection of a dairy herd with bovine viral diarrhea virus. Prev Vet Med 72, 177-181.
Voges H., Nash M., Totter T. The impact of herd exposure to BVD on somatic cell count levels and regional variation of BVD exposure amongst herds in New Zealand. Proceedings from: ESVV Pestivirus Symposium; September 16–19, 2008; Uppsala Sweden.
Kirk, J. Infectious abortions in dairy cows. UC Davis Veterinary Medicine Extension. Available at: www.vetmed.ucdavis.edu/vetext/INF-DA/Abortion.html. Accessed July 7, 2009.
Houe H, A Lindberg, V Moennig. 2006. Test strategies in bovie viral diarrhea virus control and eradication campaigns in Europe. J Vet Diagn Invest 18, 427-436.
Fux RG, RG Fux. 2007. Development and evaluation of diagnostic methods for detecting bovine viral diarrhea virus in dried ear biopsy samples using antigen-ELISAs and real-time RT-PCR [dissertation].University of Munich Veterinary Department, Munich, Germany.
Andrews JM, AD Langmuir. 1963. The philosophy of disease eradication. Am J Publ Hlth 53, 1-6.
EU Thematic network on control of bovine viral diarrhoea virus (BVDV) BVDV Control QLRT – 2001-01573.
Chi J., VanLeeuwen J.A., Weersink A., Keefe GP. Direct production losses and treatment costs from bovine viral diarrhea virus, bovine leukosis virus, Mycobacterium avium subspecies paratuberculosis, and Neospora caninum. Prev Vet Med. 2002;55(2):137–53.
Duffell S.J., Sharp M.W., Bates D. Financial loss resulting from BVD-MD virus infection in a dairy herd. The Veterinary Record. 1986;118(2):38–39.
Houe H. epidemiological features and economical importance of bovine virus diarrhoea virus (BVDV) infections. Vet Microbiol. 1999;64(2–3):89–107.
Ridpath J. Why BVD is a tough problem. Hoard’s Dairyman. October 25, 2002; 697.
Wentink G.H., Dijkhuizen A.A. Economic consequences of an infection with the bovine diarrhea virus (BVD virus) in 15 dairy farms. Tijdschr Diergeneeskd. 1990;115(22):1031–1040.










